慢性疲劳综合征(专业版)
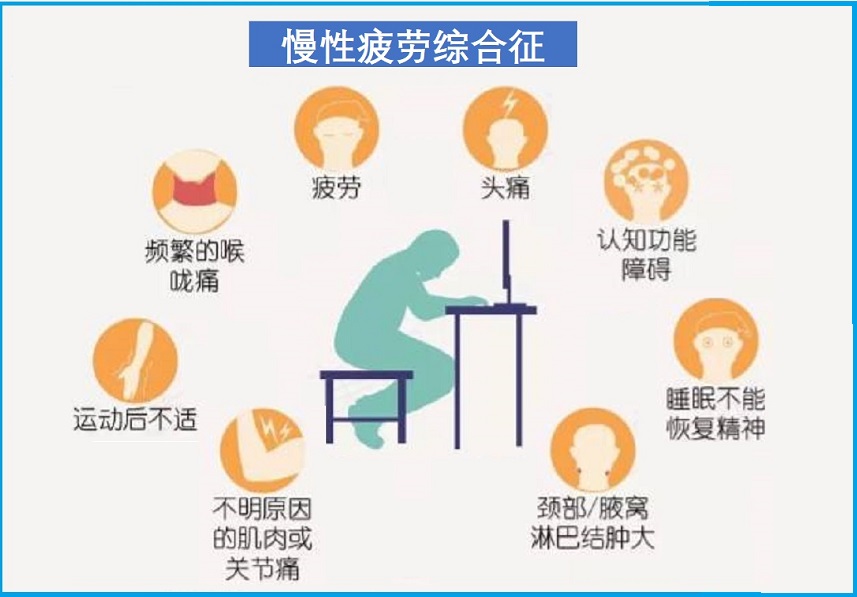
慢性疲劳综合征(CFS)是一类复杂的健康状况,其特征是深度疲劳持续六个多月以上,表现特征为肌肉和关节疼痛、情绪抑郁、认知困难和睡眠紊乱等,可影响到日常生活和工作等。
英文名称:Chronic Fatigue Syndrome,CFS
定义
慢性疲劳综合征(CFS)是一类复杂的健康状况,其特征是深度疲劳持续六个多月以上,表现特征为肌肉和关节疼痛、情绪抑郁、认知困难和睡眠紊乱等,可影响到日常生活和工作等。这种慢性、衰弱性疲劳,卧床休息缓解不了,其他疾病也都无法解释。病因
CFS的确切原因是未知的。研究认为存在下列触发因素:- 病毒感染:有些人在病毒感染后出现慢疲征,包括疱疹病毒、肠道病毒等,但尚未找到确立的关系。
- 神经-内分泌异常:荷尔蒙失衡,下丘脑-垂体-肾上腺体内产生异常血液水平的激素等。
- 免疫系统问题,如超敏反应、炎症水平和线粒体功能障碍等。
风险因素
女性比男性患CFS较为普遍,25-55岁群体较易发生。其他可能增加CFS发病的因素,包括如下:
- 最近的经历:
- 病毒感染:包括爱泼斯坦病毒(EBV)、多种肠道病毒,风疹(德国麻疹)等。
- 细菌感染
- 真菌或酵母感染
- 免疫系统受到抑制
- 长期压力、慢性应激
- 自体免疫反应
- 过敏或超敏反应,对食品、化学品、气味、药物和光线等
- 接触毒素
- 创伤
症状
CFS症状因人而异,可能包括如下:- 衰弱性疲劳,原因不明且卧床休息不能缓解,身体或脑活动后加重
- 不明原因的肌肉酸痛
- 关节痛,超过6个月但没有红肿·
- 头痛6个月以上
- 短期记忆或集中精力困难
- 健忘失忆或思维混乱
- 烦躁、焦虑、恐慌,情绪波动、或抑郁
- 喉咙痛超过6个月
- 淋巴结不适超过6个月
- 睡眠困难或睡眠后难恢复,超过6个月
- 视力问题,如模糊或眼痛
- 社会活动减少,工作、教育和个人
- 头晕,平衡问题或晕厥
- 发冷、晚上盗汗
疗法
CFS是无法治愈的,但可对它的症状治疗和控制,以改善生活质量。采用综合疗法可能是最有效的,选项包括如下:调整饮食和生活方式
- 健康、均衡饮食,富含蔬菜、水果和全谷类食物等
- 不要吸烟,或戒烟
- 避免接触有毒化学品、污染源等
- 经常运动锻炼,提高免疫力
- 学会和运用压力管理
- 睡眠充足、劳逸结合
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控慢疲征的营养和草本补充剂,主要包括如下:
1.线粒体靶向支持:
线粒体是细胞的能量来源,以ATP的形式产生化学能。ATP为全身细胞反应提供“燃料”。因此,在能量减少或疲劳的情况下,支持线粒体功能可能是有益的,包括慢性疲劳综合征1,2。
1.1.辅酶Q10:
辅酶Q10(CoQ10)是线粒体产生细胞能量分子(ATP)过程中的一个关键因素3。辅酶Q10存在于肉类中,并在人体内合成量很少,但在健康人的线粒体中含量丰富4。一项针对58名CFS患者的研究报告称,高达45%的患者血液中辅酶Q10水平低于正常水平,而22名健康对照者的血液中辅酶Q10水平均低于正常水平。与CoQ10水平较高的CFS患者相比,CoQ10水平极低的CFS患者在疲劳、注意力和记忆方面的问题明显更多3。
单独使用CoQ10或与脱氢酶(NADH)联合使用已被证明可以减轻疲劳并提高纤维肌痛和CFS的运动耐受性5,6。一项针对纤维肌痛症患者的随机对照试验报告,与10名安慰剂治疗的纤维肌痛患者相比,10名每天三次服用100mg CoQ10持续40天,受试者的疲劳、疼痛和压痛点水平明显降低7。
1.2.烟酰胺腺嘌呤二核苷酸(NAD):
NAD是无数生理过程中的关键辅助因子,在体内由烟酸(维生素B3)制成8。在一项针对20名CFS患者的随机开放标签试验中,12名受试者每天口服5mg 脱氢酶(NADH,一种NAD);如果症状没有改善,则增加到10mg,8名受试人员接受了包括心理治疗在内的综合计划。三个月后NADH组的平均CFS症状评分显著降低,尽管后来的测量发现两种治疗方法是可比较的9。
另一项对26名符合美国CDC CFS标准的受试者的研究报告称,31%的人对四周每天补充10mg NADH的反应良好,而安慰剂的这一比例为8%10。一项随机对照试验将NADH与CoQ10联合使用,既支持线粒体功能,并在CFS中具有临床前景。在这项试验中,73名被诊断为CFS的女性在8周内每天接受200mg辅酶Q10加20mg NADH或安慰剂治疗。在补充前进行基线测量,并在第8周结束时再次进行基线测量。通过评估问卷报告,与安慰剂相比,补充剂可显著提高ATP的产生水平,并显著改善疲劳水平。
NADH是NAD+的还原形式,在不可或缺的能量产生细胞过程中,两者作为电子传输链的一部分定期相互转化。除了在ATP生成中的作用外,NAD+对Sirtuins也是必不可少的,Sirtuins是一种专门的蛋白质,可以防止DNA损伤,并有助于缓解与年龄相关的下降11。这一过程依赖于NAD+的健康供应12。不幸的是,NAD+水平会随着年龄的增长而下降11。好消息是,烟酰胺核糖(NR)、β-烟酰胺单核苷酸(NMN)等化合物可以提高NAD+水平13。
1.3.肉碱:
L-肉碱是一种氨基酸衍生物,通过帮助脂肪酸运输到线粒体中氧化以获取能量,在能量生产中发挥重要作用。L-肉碱在能量和细胞代谢中还有其他几个重要作用14,15。二项研究报告称,与对照组相比,CFS患者的血液肉碱和酰基肉碱显著降低16,17。在第二项研究中,血液肉碱水平越高,临床状况越好。一项针对30名CFS受试者的为期两个月的研究比较了抗甲型流感的抗病毒药物金刚烷胺(Symmetrel)和L肉碱。金刚烷胺耐受性差,没有任何显著改善。补充L-肉碱耐受性良好,在18项测量的临床参数中有12项显著改善,治疗第二个月改善最大18。
另一组研究人员在一项开放标签试验中治疗90名CFS患者(每组30人),分别使用2g乙酰L肉碱、2g丙酰L肉碱或每天各2g(共4g)。治疗24周后,乙酰L肉碱组、丙酰L肉碱组和联合组分别有59%、63%和37%的受试者出现了显著改善(以临床总体印象评分衡量)。乙酰L肉碱对精神疲劳和注意力集中等脑功能有显著影响,而丙酰L肉碱对全身疲劳和身体疲劳的改善效果最大19。
乙酰L肉碱作为CFS试验的一部分,该试验同时使用了针对线粒体功能的营养品和低剂量哌甲酯。在该研究中,与安慰剂相比,试验组在疲劳和疼痛方面表现出明显更好的临床反应20。
肉碱也可能对其他导致长期疲劳的情况有用。一项随机对照试验比较了乙酰-L-肉碱和金刚烷胺治疗36例多发性硬化症患者慢性疲劳的疗效。在90天内,每天两次服用1g 乙酰-L-肉碱的患者比每天两次使用100mg金刚烷胺的患者的疲劳严重程度明显减轻21。
2.橡木提取物(Roburins):
Roburins是法国橡木的成分,属于植物多酚类鞣花丹宁(Ellagitannins)22。Roburins已被人类在橡木桶中陈酿的葡萄酒和烈酒中消费了几个世纪。鞣花丹宁能够调节体内的炎症反应22,23。每天服用高达300mg胶囊的橡木提取物,已被证明可以改善健康成年人的精神专注力、能量水平和运动表现24,25。最近报道了一项随机、双盲、安慰剂对照的初步研究结果显示,66名接受子宫切除术的妇女在补充四周橡木提取物后,自我报告的康复结果有所改善26。
法国橡木提取物(Robuvit®,一种专有提取物)被认为具有这种作用,至少部分是因为它能够改善核糖体(Ribosomes)的功能,核糖体是一种细胞机制,负责将遗传信息转化为可用的蛋白质和肽22。核糖体失调也与CFS和慢性病毒综合征的症状有关27。
在一项评估85名CFS患者的开放标签试验中,45名患者接受了橡木提取物治疗,40名患者作为对照。在全面的医学评估以排除其他疲劳原因后,受试者被随访至少六个月。研究人员追踪了CFS患者的身体症状和情绪,以及氧化应激的测量结果。在第三个月和第六个月时,治疗组的全血氧化应激显著降低,而对照组没有显著变化28。补充橡木的组大多数CFS症状评分显著下降,尤其是在六个月后。而对照组的改善很小,或在某些情况下,三个月和六个月时症状恶化。橡木提取物被证明可以适度改善睡眠、记忆力或注意力、肌肉和关节疼痛、头痛和淋巴结肿大。在评估的9种次要症状中,对照组的症状几乎没有变化,在某些情况下,症状在3个月和6个月时恶化,而补充Roburins组对噪音、食物、药物和化学品的敏感性有统计学上的显著改善,包括头晕或头昏、抑郁、情绪波动、体重变化、过敏症状,以及视觉症状。
3.D-核糖:
核糖是一种碳水化合物,对合成重要的生物化合物至关重要,如RNA和DNA(细胞遗传物质),以及许多参与细胞能量生产和转移的化合物(如CoA、ATP、NADH和FADH)29。一项初步研究分析了36名患有CFS和/或纤维肌痛的受试者,他们每天三次服用5g D-核糖。平均治疗25天后,受试者报告疲劳明显减轻,整体健康状况改善,睡眠改善,思维清晰度提高,疼痛阈值改善30。
低水平的ATP生成被认为是CFS患者最小限度运动时疲劳的一种可能的潜在机制。在剧烈运动后的运动生理学中也观察到了类似的ATP消耗模式,D-核糖已被证明可以在这种情况下增强ATP的恢复。在一项交叉双盲研究中,26名健康受试者(平均年龄28岁)在运动前两天服用10g负荷剂量的D-核糖,然后每天补充10g,并进行为期三天的60分钟高强度训练。对照组给予改性葡萄糖(右旋糖)31。补充D-核糖后,受试者的能量输出增加,感知疲劳减少,而对照组干预没有观察到益处。
随着对能量水平恢复增强与补充D-核糖之间联系的理解,D-核糖在CFS中的有益作用值得进一步研究。
4.维生素B族:
B族维生素如:维生素B1(硫胺素)、维生素B2(核黄素)和维生素B6(吡哆醇)在体内许多能量产生反应中发挥着关键作用,而其他B族维生素,如叶酸(B9)和维生素B12(如甲钴胺),对创造新细胞、修复受损细胞和中枢神经系统的正常功能都很重要32,33。
一项研究发现,与18名年龄和性别匹配的对照组相比,12名CFS患者的维生素B1、B2,尤其是b6相关酶活性明显降低34。另一项研究报告称,60名CFS患者中有30人的血清叶酸异常低35。一项试验将安慰剂与38名18-50岁CFS女性患者的每日低效力复合维生素/矿物质补充剂进行了比较。除了其他营养素外,该补充剂还含有的B族维生素:4.2mg B1、4.8mg B2、6mg B6、54mg烟酸、600mcg叶酸和3mcg B12。两个月后,与服用安慰剂的女性相比,服用该补充剂的女性明显减轻了疲劳,改善了睡眠,剧烈头痛也减轻了36。据报道,一种多营养静脉注射营养配方被称为“梅尔鸡尾酒(Myer’s cocktail)”,其中包括B族维生素、镁和其他营养素,可以帮助CFS患者37。
2019年的一项研究考察了高剂量的维生素B12鼻腔滴注对CFS患者的疗效。治疗为5000 mcg羟钴胺素,每周两次。三分之二的滴鼻者对治疗有反应,表现出身体活动和疲劳水平的显著改善,血清B12水平也显著升高38。另一方面,本研究中的无反应者在治疗后表现出疲劳和活动水平改善,甚至在B12水平方面也表现出微小的改善。
5.益生菌:
胃肠道症状是CFS的常见症状,胃肠道屏障功能障碍是CFS免疫失调的可能机制。多样化和平衡的肠道菌群对健康的肠道屏障至关重要,但据报道,CFS患者肠道菌群缺乏生物多样性和失衡39。这为在慢性疲劳综合症中使用益生菌提供了合理的理由。
一些研究发现,益生菌如乳酸菌和双歧杆菌,可以减轻CFS症状。意大利的一项研究报告称,13名CFS患者在接受包括双歧杆菌和乳酸杆菌在内的各种组合益生菌治疗8周后,疲劳程度逐渐改善,炎症生物标志物显著减少40。一项针对29名60-81岁健康成年人的对照试验报告称,每天食用100g含有活菌的发酵乳饮料与不含益生菌的安慰剂饮料相比,三周的瑞士乳杆菌显著改善了睡眠41。
一项针对15名符合1994年美国CDC CFS标准的受试者的研究报告称,用副干酪乳杆菌、嗜酸乳杆菌和乳双歧杆菌治疗30天,每天二次,减少了40%受试者与CFS相关的神经认知症状42。在一项针对CFS益生菌的安慰剂对照试验研究中,39名成年人服用了含有80亿活干酪乳杆菌的益生菌混合物,连续两个月,每天三次。与安慰剂相比,治疗显著降低了焦虑43。
然而,最近的一些系统综述表明,益生菌对CFS有益的证据有限,且不具有严格的方法学质量44,45。因此,需要在CFS患者中进行更大规模的益生菌对照试验。
6.镁:
镁是参与人类数百种酶反应的必需矿物质,其缺乏可能与慢性疲劳有关46。镁摄入不足是一个常见且经常被低估的问题47。例如,2013-2016年美国国家健康与营养调查(NHANES)的一项数据分析发现,49%的所有年龄段的美国人从食品和饮料中摄入的镁少于他们估计的平均需求量,即30岁以上的男性和女性分别为每天420mg和320mg48。
一些(但不是全部)研究报告称,补充镁对CFS或纤维肌痛患者有帮助。为了测试镁在慢性疲劳综合征中的作用,研究人员在一项单独的研究中首次报告,与20名健康对照组相比,20名患有CFS的成年人红细胞镁水平显著降低,并在一项安慰剂对照临床试验中进行了随访。在该试验中,32名CFS患者被随机选择每周肌肉注射1g硫酸镁(15名患者)或安慰剂(17名患者)持续6周49。治疗组的能量水平显著提高,疼痛减轻,情绪反应减轻,与安慰剂相比,总体改善显著。80%接受镁治疗的受试者报告从治疗中获益,而对照组为18%。尽管不是CFS研究,但一项对24名纤维肌痛受试者进行的每日高达600mg镁和2400mg苹果酸的非对照试验报告称,疼痛和压痛明显下降50。
镁含量可以通过多种方式测量。其中包括红细胞镁、血清镁,有时还有24小时尿镁。传统的镁测试可能会被误解,因为标准正常范围包括次优水平和亚临床镁缺乏51,52。这在一些测试血清镁并得出镁状态足够的结论的研究中造成了混乱。红细胞和血清镁必须正确解释,正确理解真正的最佳和亚临床缺乏水平。
7.维生素D:
维生素D在免疫、肌肉骨骼、心血管和内分泌功能中发挥着关键作用53。鉴于维生素D在身体中的多种作用,维生素D与CFS有关也就不足为奇了。
一项针对221名CFS患者的研究表明,平均维生素D血液水平低于18ng/mL,显著低于对照组54。另一项针对41名CFS患者的研究发现,维生素D水平与心血管风险、炎症和氧化应激的一些生物标志物呈负相关,包括TNF-α、异前列腺素和臂舒张压55。在这项研究中,受试者的维生素D水平同样较低,中位水平仅为18ng/mL。
其他研究人员认为,维生素D可能通过调节与CFS有关的炎症途径,即核因子κB(NF-κB)途径,对改善慢性疲劳综合症有用。维生素D的活性代谢产物1,25-二羟基维生素D抑制NF-κB通路的激活,NF-κB通路驱动炎症,其慢性激活与CFS症状有关56。
8.维生素C:
氧化应激,特别是在运动后,可能会导致慢性疲劳。在一项包括38名CFS患者和5名健康对照的研究中,20名有严重急性感染史(腹膜炎、肺炎、急性呼吸窘迫综合征或脑脊髓炎)的CFS患者的抗坏血酸(体内可作为抗氧化剂的维生素C形式)水平低于对照组。这项研究还发现,在最大限度的运动循环测试后,与对照受试者相比,有高水平运动史或严重急性感染史的CFS患者的氧化应激标志物(TBARS)升高57。在另一项研究中,与健康受试者相比,慢性疲劳综合征患者的抗坏血酸与TBARS的比例更低58。在其他研究中发现,在相同强度的运动后,CFS参与者的抗坏血酸氧化几乎是健康人的三倍59。总之,这些发现表明,一些CFS患者可能对维生素C的需求增加,尤其是在运动过程中。
维生素C可能对患有EB病毒感染的CFS患者有益。一份基于218名EB病毒感染患者(其中110名患有CFS)数据的临床报告发现,较高的维生素C水平与较低的EB病毒抗体水平相关,每次7.5–50g的静脉注射维生素C治疗,可显著降低EBV抗体水平。此外,那些接受了五次或五次以上静脉注射维生素C治疗的人,其EBV抗体水平的下降幅度比其他没有接受任何静脉注射维生素C的人明显更大、更快60。不幸的是,该研究没有报告疲劳水平的变化。
9. 欧米伽3脂肪酸:
DHA和EPA等Omega-3脂肪酸在鱼油和磷虾油等海洋油脂中含量丰富,可调节体内的炎症途径。它们对支持细胞膜的完整性也很重要,并可对血脂水平产生有利影响61。
体内低ω-3水平与促炎状态和心血管风险增加有关。2018年一项针对西班牙31名CFS患者的横断面研究发现,绝大多数参与者的DHA和EPA水平较低62。这些发现证实了CFS患者早期类似的低ω-3水平发现63。
在一项针对63名患有病毒后疲劳综合征的成年人的研究中,受试者每天接受4g剂量的ω-6脂肪酸和鱼油的混合物治疗,或接受匹配的安慰剂治疗。在三个月时,85%的治疗组报告显著改善,而安慰剂组为17%64。一项针对4名CFS受试者的非对照研究发现,每天补充高EPA配方12周后,所有受试者的症状都得以改善65。
10.褪黑素:
褪黑素调节睡眠-觉醒周期,且是一种有效的抗氧化剂66。对14项已发表研究的分析表明,睡前服用褪黑素可显著降低延迟睡眠期综合征患者的睡眠潜伏期(入睡时间)67。在一项针对29名患有慢性疲劳至少12个月的CFS患者的非对照试验中,受试者每天服用5mg褪黑素。经过三个月的治疗,受试者在疲劳、注意力和活动的标准化评估中的得分都显著改善。在治疗期间,8名受试者的过度疲劳完全消除68。
帕金森病患者经常出现慢性持续疲劳,符合CFS的诊断标准。在一项针对30名有CFS症状的帕金森患者的研究中,褪黑素治疗显著降低了标准化帕金森评估中的疲劳和焦虑评分,并改善了生活质量;褪黑素治疗后睡眠质量也有所改善69。根据截至2020年年中的现有证据,对CFS患者进行更大规模的、随机的、对照的褪黑素补充试验是合适的。
11.姜黄素:
姜黄是一种富含多酚姜黄素的香料70。荷兰的一项开放标签研究观察了44名CFS患者补充姜黄素的益处71。受试者每天服用与胆碱复合的姜黄素植物体,持续8周,并被要求在干预开始前和干预结束时填写CFS症状调查表。受试者报告疲劳、睡眠障碍和疼痛评分显著降低。
众所周知,纯姜黄素的生物利用度很低,这意味着只有一小部分被吸收,而大部分被吸收的物质被代谢并转化为其他形式72。科学家可能已经找到了一种解决方案,通过将姜黄素与胡芦巴中发现的一种名为“半乳甘露聚糖”的化合物相结合,可以显著提高姜黄素的生物利用度73。在一项随机双盲交叉试验中,对50名健康人进行了研究74。结果显示,与未共轭的纯姜黄素相比,共轭配方使活性游离姜黄素在血液中的含量高出45倍。从那时起,使用该配方进行了更多的研究,包括一项随机对照试验,以测试60名患有职业压力相关焦虑和疲劳的受试者的疗效,其中256人接受了姜黄内酯甘露糖苷(Curcumagalactomannoside)配方,剂量为500mg,每天两次。通过使用生活质量指标,研究人员报告了焦虑、压力和疲劳水平的显著改善。
12.可可:
巧克力由可可豆制成,可可豆含有多种植物化学物质(如多酚和其他黄酮类化合物),具有多种健康益处,包括可能降低心血管疾病和癌症的风险。黑巧克力可能在治疗CFS中发挥作用。
一项研究使用15g富含多酚的黑巧克力治疗10名患有慢性疲劳综合征的成年人,每天三次。经过八周的治疗,疲劳、抑郁和焦虑的得分显著下降。然后,在两周的无治疗期后,参与者被给予另一种制剂,即15g低多酚模拟黑巧克力,每天三次。在此期间,他们的病情明显恶化。模拟黑巧克力除了多酚含量较低外,还有其他差异;它含有全脂奶粉(活性治疗组不含),糖的百分比几乎是活性治疗组的两倍,碳水化合物的百分比超过活性治疗组的二倍多75。
巧克力中的化合物可能与大脑中的各种受体相互作用76,并表明CFS受试者的神经递质失衡77。研究人员推测,通过调节神经递质,富含多酚的巧克力可以减轻CFS的症状75。应对高酚类食物和饮食进行更多研究,以证实这些在慢性疲劳综合症中的发现。
13.磷脂酰胆碱和胆碱:
磷脂酰胆碱是细胞膜的主要成分,有助于脂肪代谢,也是必需营养素胆碱的来源,胆碱本身是甲基供体甜菜碱(三甲基甘氨酸)和神经递质乙酰胆碱的前体78,79。与健康对照组相比,CFS患者的血液中磷脂酰胆碱水平较低80,81。有人提出,补充磷脂酰胆碱和其他细胞膜组分加抗氧化剂可以增强对CFS患者的氧化应激和改善细胞和线粒体功能82,83。
一项开放标签试验发现,15名中度至重度慢性疲劳受试者在使用含有膜脂质、益生菌以及各种营养素等专利补充剂4至8周后,线粒体功能更好,疲劳减轻83。在另一项针对58名慢性疲劳参与者(其中30人患有CFS)的开放标签试验中,用相同的补充剂以及提供维生素E、NADH、辅酶Q10、钙、磷、镁、α-酮戊二酸、L-酪氨酸、L-肉碱、L-酒石酸盐和泛硫乙胺(一种维生素B5相关营养素)的补充剂进行治疗,导致8周后疲劳测试的分数下降了30%以上84。
除了改善细胞和线粒体功能外,胆碱还可以通过支持甲基化和毒素清除来帮助CFS患者85。据报道,胆碱和维生素C的组合可以改善4名被诊断为CFS患者的症状,这些患者被发现具有高水平的有机磷(农药环境毒素)。有机磷水平的降低与症状的改善同时发生86。
14.适应原药草:
适应原草药(Adaptogen herbs)可能改善慢性疲劳。几种药用植物显示出增强身体对精神和身体压力的整体抵抗力的非特异性能力。尽管确切的机制尚不清楚,但有证据表明,它们可能影响HPA轴和参与身体应激反应的几种生化途径87。
适应原对CFS特别有益,因为它们以增强能量而闻名,并且可能对HPA轴和支持健康免疫系统功能产生影响。一些被认为有前景用于CFS的适应原包括:
14.1.人参:
亚洲参是一种原产于亚洲(主要是中国和韩国)的多年生草本植物88。另一个品种是花旗参(即西洋参)原产于北美89。根据加工方式,人参根可能是白色或红色的。人参是一种适应性强的草本植物,被认为具有缓解疲劳的功效90,91。
在2013年的一项随机对照试验中,在一组患有不明原因慢性疲劳的个体中,将每天1g或2g剂量的人参提取物与安慰剂进行了比较,2g剂量显著减少了疲劳,改善了精神功能,减少了氧化应激92。2020年完成的双盲安慰剂对照试验显示,红参在六周内以每天3g的剂量给药,在减轻中年人中度疲劳方面具有治疗潜力93,与安慰剂相比,疲劳减轻程度明显更大。
14.2.红景天:
红景天对非CFS身心疲劳的影响已被研究,但结果不一致94。基于临床前和临床研究,有人认为红景天提取物可能有助于改善CFS患者的认知功能和注意力87。在一项随机对照试验中,比较红景天提取物与抗抑郁药舍曲林和安慰剂对重度抑郁症患者的疗效和安全性。结果显示,接受340mg红景天提取物治疗12周的组有一定疗效,但红景天的抗抑郁作用低于舍曲林组;红景天的不良作用较少95。
14.3.南非醉茄:
在印度阿育吠陀医学中作为“回春剂(Rejuvenator)”有着悠久的使用历史,被认为是一种有用而强大的适应原96。它已被研究用于影响中枢神经系统的疾病,包括压力、毒瘾和神经退行性疾病,如帕金森病和阿尔茨海默病97。虽然没有在CFS中进行专门研究,但在接受化疗的乳腺癌患者队列中研究了南非醉茄对疲劳的影响98。在这项开放性病例对照试验中,50名受试者接受了2g胶囊形式的南非醉茄提取物,与对照组中未接受南非醉茄的50名化疗受试者相比,在六个周期的化疗中每天三次的受试者报告的疲劳明显减轻。
更多关于适应原药草相关内容,可参阅本网专文:慢性压力管理 >>
更多内容可点击其个性化综合干预方案如下:
不同性别、年龄段的慢疲症干预方案:
以及参阅本网如下专文的相关内容:
医疗干预
常规用于治疗CFS症状的药物包括:
- 抗抑郁药
- 抗焦虑药
- 非处方药,如布洛芬和对乙酰氨基酚
- 温和的兴奋剂
- 镇静剂,改善失眠
其他疗法
一些疗法可缓解CFS症状如:
- 理疗或替代疗法,如:按摩、拉伸、瑜伽和太极等··
- 防止食物过敏:CFS患者对某些食物易过敏。
- 心理治疗,主要如下:
- CFS可导致身心衰弱,抑郁在CFS患者中也很常见,心理治疗可帮助应对。
- 学习放松训练和压力管理,以及改变睡眠习惯可缓解症状。
- 认知行为疗法(CBT) 也可能减少疲劳症状。CBT能帮助改变患者对环境的感知和反应,特别是那些超出控制能力的情况。
预防
因为原因不明,目前没有预防CFS的指南。
参考文献:
1. Wawrzyniak NR et al. Idiopathic chronic fatigue in older adults is linked to impaired mitochondrial content and biogenesis signaling in skeletal muscle. Oncotarget. Aug 16 2016;7(33):52695-52709.
2. Nicolson GL. Mitochondrial Dysfunction and Chronic Disease: Treatment With Natural Supplements. Integrative medicine (Encinitas, Calif). Aug 2014;13(4):35-43.
3. Maes M et al. Coenzyme Q10 deficiency in myalgic encephalomyelitis/chronic fatigue syndrome (ME/CFS) is related to fatigue, autonomic and neurocognitive symptoms and is another risk factor explaining the early mortality in ME/CFS due to cardiovascular disorder. Neuro endocrinology letters . 2009;30(4):470-6.
4. Molyneux SL et al. Coenzyme Q10: is there a clinical role and a case for measurement? The Clinical biochemist Reviews. 2008;29(2):71-82.
5. Morris G et al. Coenzyme Q10 depletion in medical and neuropsychiatric disorders: Potential repercussions and therapeutic implications. Humana Press Inc.; 2013. p. 883-903.
6. Castro-Marrero J et al. Effect of coenzyme Q10 plus nicotinamide adenine dinucleotide supplementation on maximum heart rate after exercise testing in chronic fatigue syndrome - A randomized, controlled, double-blind trial. Clin Nutr. Aug 2016;35(4):826-34.
7. Cordero MD et al. Can coenzyme q10 improve clinical and molecular parameters in fibromyalgia? Antioxid Redox Signal. Oct 20 2013;19(12):1356-61.
8. Higdon J. Oregon State University. Niacin: Function. Updated 12/2017. Accessed 12/15/2020, https://lpi.oregonstate.edu/mic/vitamins/niacin#function
9. Santaella ML et al. Comparison of oral nicotinamide adenine dinucleotide (NADH) versus conventional therapy for chronic fatigue syndrome. P R Health Sci J. Jun 2004;23(2):89-93.
10. Forsyth LM et al. Therapeutic effects of oral NADH on the symptoms of patients with chronic fatigue syndrome. Ann Allergy Asthma Immunol. Feb 1999;82(2):185-91.
11. Lee SH et al. Sirtuin signaling in cellular senescence and aging. BMB reports. Jan 2019;52(1):24-34.
12. Anderson RM et al. Nicotinamide and PNC1 govern lifespan extension by calorie restriction in Saccharomyces cerevisiae. Nature. May 8 2003;423(6936):181-5.
13. Dolopikou CF et al. Acute nicotinamide riboside supplementation improves redox homeostasis and exercise performance in old individuals: a double-blind cross-over study. European journal of nutrition. Mar 2020;59(2):505-515.
14. Sharma S et al. CARNITINE HOMEOSTASIS, MITOCHONDRIAL FUNCTION, AND CARDIOVASCULAR DISEASE. Drug Discov Today Dis Mech. 2009;6(1-4):e31-e39.
15. Higdon J. Oregon State University. L-Carnitine. Updated 7/2019. Accessed 12/15/2020, https://lpi.oregonstate.edu/mic/dietary-factors/L-carnitine
16. Kuratsune H et al. Acylcarnitine deficiency in chronic fatigue syndrome. Clinical infectious diseases : an official publication of the Infectious Diseases Society of America . Jan 1994;18 Suppl 1(Supplement_1):S62-7.
17. Plioplys AV et al. Serum levels of carnitine in chronic fatigue syndrome: clinical correlates. Neuropsychobiology. 1995;32(3):132-8.
18. Plioplys AV et al. Amantadine and L-carnitine treatment of Chronic Fatigue Syndrome. Neuropsychobiology. 1997;35(1):16-23.
19. Vermeulen RC et al. Exploratory open label, randomized study of acetyl- and propionylcarnitine in chronic fatigue syndrome. Psychosomatic medicine. Mar-Apr 2004;66(2):276-82.
20. Montoya JG et al. KPAX002 as a treatment for Myalgic Encephalomyelitis/Chronic Fatigue Syndrome (ME/CFS): a prospective, randomized trial. International Journal of Clinical and Experimental Medicine. 2018;11(3):2890-2900.
21. Tomassini V et al. Comparison of the effects of acetyl L-carnitine and amantadine for the treatment of fatigue in multiple sclerosis: results of a pilot, randomised, double-blind, crossover trial. J Neurol Sci. Mar 15 2004;218(1-2):103-8. 05
22. Natella F et al. Absorption, metabolism, and effects at transcriptome level of a standardized French oak wood extract, Robuvit, in healthy volunteers: pilot study. J Agric Food Chem. Jan 15 2014;62(2):443-53.
23. Piwowarski JP et al. Influence of gut flora-derived ellagitannins' metabolites- urolithins on production and release of pro-inflammatory factors from stimulated neutrophils in the context of cardiovascular disease prevention. Planta Medica. 2013;79(13)
24. Orszaghova Z et al. An Effect of Oak-Wood Extract (Robuvit(R)) on Energy State of Healthy Adults-A Pilot Study. Phytother Res. Aug 2015;29(8):1219-24.
25. Vinciguerra MG et al. Robuvit® and endurance in triathlon: improvements in training performance, recovery and oxidative stress. Minerva cardioangiologica. 2015;63(5):403-9.
26. Ferianec V et al. The Oak-wood Extract Robuvit((R)) Improves Recovery and Oxidative Stress after Hysterectomy: A Randomized, Double-blind, Placebo-controlled Pilot Study. Nutrients. Mar 27 2020;12(4):913-913.
27. Bhavsar RB et al. The other lives of ribosomal proteins. Hum Genomics. Jun 2010;4(5):327-44.
28. Belcaro G et al. Improved management of primary chronic fatigue syndrome with the supplement French oak wood extract (Robuvit®): a pilot, registry evaluation. Panminerva medica. Mar 2014;56(1):63-72.
29. Dhanoa TS et al. Ribose: more than a simple sugar? Current sports medicine reports. Jul 2007;6(4):254-7.
30. Teitelbaum JE et al. The use of D-ribose in chronic fatigue syndrome and fibromyalgia: a pilot study. Journal of alternative and complementary medicine (New York, NY). Nov 2006;12(9):857-62.
31. Seifert JG et al. The influence of D-ribose ingestion and fitness level on performance and recovery. Journal of the International Society of Sports Nutrition. 2017;14:47.
32. Woolf K et al. B-vitamins and exercise: does exercise alter requirements? International journal of sport nutrition and exercise metabolism. Oct 2006;16(5):453-84.
33. Reynolds E. Vitamin B12, folic acid, and the nervous system. Lancet Neurol. Nov 2006;5(11):949-60.
34. Heap LC et al. Vitamin B status in patients with chronic fatigue syndrome. J R Soc Med. Apr 1999;92(4):183-5.
35. Jacobson W et al. Serum folate and chronic fatigue syndrome. Neurology. Dec 1993;43(12):2645-7.
36. Maric D et al. Multivitamin mineral supplementation in patients with chronic fatigue syndrome. Med Sci Monit. Jan 14 2014;20:47-53.
37. Gaby AR. Intravenous nutrient therapy: the 'Myers' Cocktail'. Alternative Medicine Review. 2002 Oct;7(5):389-403.
38. van Campen CLM et al. Open Trial of Vitamin B12 Nasal Drops in Adults With Myalgic Encephalomyelitis/Chronic Fatigue Syndrome: Comparison of Responders and Non-Responders. Frontiers in pharmacology. 2019;10(SEP):1102.
39. Giloteaux L et al. Reduced diversity and altered composition of the gut microbiome in individuals with myalgic encephalomyelitis/chronic fatigue syndrome. Microbiome. Jun 23 2016;4(1):30.
40. Venturini L et al. Modification of Immunological Parameters, Oxidative Stress Markers, Mood Symptoms, and Well-Being Status in CFS Patients after Probiotic Intake: Observations from a Pilot Study. Oxid Med Cell Longev. 2019;2019:1684198.
41. Yamamura S et al. The effect of Lactobacillus helveticus fermented milk on sleep and health perception in elderly subjects. European journal of clinical nutrition. Jan 2009;63(1):100-5.
42. Sullivan A et al. Effect of supplement with lactic-acid producing bacteria on fatigue and physical activity in patients with chronic fatigue syndrome. Nutr J. Jan 26 2009;8(1):4.
43. Rao AV et al. A randomized, double-blind, placebo-controlled pilot study of a probiotic in emotional symptoms of chronic fatigue syndrome. Gut Pathogens. Mar 19 2009;1(1):6.
44. Corbitt M et al. A Systematic Review of Probiotic Interventions for Gastrointestinal Symptoms and Irritable Bowel Syndrome in Chronic Fatigue Syndrome/Myalgic Encephalomyelitis (CFS/ME). Probiotics and antimicrobial proteins. Sep 2018;10(3):466-477.
45. Roman P et al. Are probiotic treatments useful on fibromyalgia syndrome or chronic fatigue syndrome patients? A systematic review. Benef Microbes. Jun 15 2018;9(4):603-611.
46. Cuciureanu MD et al. Magnesium and stress. In: Vink R, Nechifor M, eds. Magnesium in the Central Nervous System. University of Adelaide Press © 2011 The Authors.; 2011.
47. Rosanoff A et al. Suboptimal magnesium status in the United States: are the health consequences underestimated? Nutrition reviews. Mar 2012;70(3):153-64.
48. USDA. United States Department of Agriculture. Unusual Nutrient Intake from Food and Beverages, by Gender and Age, What We Eat in America, NHANES 2013-2016. Updated 5/2019. Accessed 10/22/2020, https://www.ars.usda.gov/ARSUserFiles/80400530/pdf/usual/Usual_Intake_gender_WWEIA_2013_2016.pdf
49. Cox IM et al. Red blood cell magnesium and chronic fatigue syndrome. Lancet. Mar 30 1991;337(8744):757-60.
50. Russell IJ et al. Treatment of fibromyalgia syndrome with Super Malic: a randomized, double blind, placebo controlled, crossover pilot study. The Journal of rheumatology. May 1995;22(5):953-8.
51. Costello RB et al. Interpreting magnesium status to enhance clinical care: key indicators. Current opinion in clinical nutrition and metabolic care. Nov 2017;20(6):504-511.
52. Costello RB et al. Perspective: The Case for an Evidence-Based Reference Interval for Serum Magnesium: The Time Has Come. Advances in Nutrition: An International Review Journal. November 1, 2016 2016;7(6):977-993.
53. Higdon J. Oregon State University. Vitamin D. Updated 7/2017. Accessed 12/17/2020, https://lpi.oregonstate.edu/mic/vitamins/vitamin-D
54. Berkovitz S et al. Serum 25-hydroxy vitamin D levels in chronic fatigue syndrome: a retrospective survey. International journal for vitamin and nutrition research. Jul 2009;79(4):250-4.
55. Witham M et al. Association between vitamin D status and markers of vascular health in patients with chronic fatigue syndrome/myalgic encephalomyelitis (CFS/ME). Int J Cardiol. Jun 1 2014;174(1):139-40.
56. Hoeck AD et al. Will vitamin D supplementation ameliorate diseases characterized by chronic inflammation and fatigue? Med Hypotheses. Feb 2011;76(2):208-13.
57. Jammes Y et al. Chronic fatigue syndrome: acute infection and history of physical activity affect resting levels and response to exercise of plasma oxidant/antioxidant status and heat shock proteins. J Intern Med. Jul 2012;272(1):74-84.
58. Fenouillet E et al. Association of biomarkers with health-related quality of life and history of stressors in myalgic encephalomyelitis/chronic fatigue syndrome patients. Journal of translational medicine. Aug 31 2016;14(1):251.
59. Jammes Y et al. Chronic fatigue syndrome: assessment of increased oxidative stress and altered muscle excitability in response to incremental exercise. J Intern Med. Mar 2005;257(3):299-310.
60. Mikirova N et al. Effect of high dose vitamin C on Epstein-Barr viral infection. Med Sci Monit. May 3 2014;20:725-32.
61. Riediger ND et al. A systemic review of the roles of n-3 fatty acids in health and disease. J Am Diet Assoc. Apr 2009;109(4):668-79.
62. Castro-Marrero J et al. Low omega-3 index and polyunsaturated fatty acid status in patients with chronic fatigue syndrome/myalgic encephalomyelitis. Prostaglandins Leukot Essent Fatty Acids. Dec 2018;139:20-24.
63. Maes M et al. In chronic fatigue syndrome, the decreased levels of omega-3 poly-unsaturated fatty acids are related to lowered serum zinc and defects in T cell activation. Neuro endocrinology letters. Dec 2005;26(6):745-51.
64. Behan PO et al. Effect of high doses of essential fatty acids on the postviral fatigue syndrome. Acta Neurol Scand. Sep 1990;82(3):209-16.
65. Puri BK. The use of eicosapentaenoic acid in the treatment of chronic fatigue syndrome. Prostaglandins Leukot Essent Fatty Acids. Apr 2004;70(4):399-401.
66. Tordjman S et al. Melatonin: Pharmacology, Functions and Therapeutic Benefits. Curr Neuropharmacol. Apr 2017;15(3):434-443.
67. Buscemi N et al. The efficacy and safety of exogenous melatonin for primary sleep disorders. A meta-analysis. J Gen Intern Med. Dec 2005;20(12):1151-8.
68. van Heukelom RO et al. Influence of melatonin on fatigue severity in patients with chronic fatigue syndrome and late melatonin secretion. European journal of neurology. Jan 2006;13(1):55-60.
69. Datieva V et al. [The use of melatonin in the treatment of chronic fatigue syndrome and circadian rhythm disorders in Parkinson's disease.]. Zhurnal nevrologii i psikhiatrii imeni SS Korsakova. 2013;113:77-81.
70. Salehi B et al. The therapeutic potential of curcumin: A review of clinical trials. European journal of medicinal chemistry. Feb 1 2019;163:527-545.
71. van Campen CMC et al. The Effect of Curcumin on Patients with Chronic Fatigue Syndrome/Myalgic Encephalomyelitis: An Open Label Study. International Journal of Clinical Medicine. 2018;09(05):356-366.
72. Nelson KM et al. The Essential Medicinal Chemistry of Curcumin. J Med Chem. Mar 9 2017;60(5):1620-1637.
73. Pandaran Sudheeran S et al. Safety, Tolerance, and Enhanced Efficacy of a Bioavailable Formulation of Curcumin With Fenugreek Dietary Fiber on Occupational Stress: A Randomized, Double-Blind, Placebo-Controlled Pilot Study. Journal of clinical psychopharmacology. Jun 2016;36(3):236-43.
74. Kumar D et al. Enhanced bioavailability and relative distribution of free (unconjugated) curcuminoids following the oral administration of a food-grade formulation with fenugreek dietary fibre: A randomised double-blind crossover study. Journal of Functional Foods. 2016/04/01/ 2016;22:578-587.
75. Sathyapalan T et al. High cocoa polyphenol rich chocolate may reduce the burden of the symptoms in chronic fatigue syndrome. Nutr J. Nov 22 2010;9(1):55.
76. di Tomaso E et al. Brain cannabinoids in chocolate. Nature. Aug 22 1996;382(6593):677-8.
77. Parker AJ et al. The neuroendocrinology of chronic fatigue syndrome and fibromyalgia. Psychol Med. Nov 2001;31(8):1331-45.
78. Li Z et al. Phosphatidylcholine and choline homeostasis. Journal of lipid research. Jun 2008;49(6):1187-94.
79. Wiedeman AM et al. Dietary Choline Intake: Current State of Knowledge Across the Life Cycle. Nutrients. Oct 16 2018;10(10)
80. Nagy-Szakal D et al. Insights into myalgic encephalomyelitis/chronic fatigue syndrome phenotypes through comprehensive metabolomics. Sci Rep. Jul 3 2018;8(1):10056.
81. Naviaux RK et al. Metabolic features of chronic fatigue syndrome. Proc Natl Acad Sci U S A. Sep 13 2016;113(37):E5472-80.
82. Nicolson GL et al. Clinical Uses of Membrane Lipid Replacement Supplements in Restoring Membrane Function and Reducing Fatigue in Chronic Diseases and Cancer. Discoveries (Craiova). Feb 18 2016;4(1):e54.
83. Nicolson GL et al. Lipid Replacement and Antioxidant Nutritional Therapy for Restoring Mitochondrial Function and Reducing Fatigue in Chronic Fatigue Syndrome and Other Fatiguing Illnesses. Journal of Chronic Fatigue Syndrome. 2006/01/01 2006;13(1):57-68.
84. Nicolson GL et al. Lipid Replacement Therapy with a Glycophospholipid Formulation with NADH and CoQ10 Significantly Reduces Fatigue in Intractable Chronic Fatiguing Illnesses and Chronic Lyme Disease Patients. International Journal of Clinical Medicine. 2012;Vol.03No.03:8. 19382.
85. Brown BI. Chronic fatigue syndrome: a personalized integrative medicine approach. Alternative therapies in health and medicine. Jan-Feb 2014;20(1):29-40.
86. Richardson J. Four Cases of Pesticide Poisoning, Presenting as “ME,” Treated with a Choline and Ascorbic Acid Mixture. Journal of Chronic Fatigue Syndrome. 2000/01/01 2000;6(2):11-21.
87. Panossian A et al. Evidence-based efficacy of adaptogens in fatigue, and molecular mechanisms related to their stress-protective activity. Current clinical pharmacology. Sep 2009;4(3):198-219.
88. Kim JA et al. Sterols isolated from seeds of Panax ginseng and their antiinflammatory activities. Pharmacognosy magazine. Apr 2013;9(34):182-5.
89. Baeg IH et al. The world ginseng market and the ginseng (Korea). J Ginseng Res. Mar 2013;37(1):1-7.
90. Lee NH et al. Safety and tolerability of Panax ginseng root extract: a randomized, placebo-controlled, clinical trial in healthy Korean volunteers. Journal of alternative and complementary medicine (New York, NY). Nov 2012;18(11):1061-9.
91. Wang J et al. Anti-fatigue activity of the water-soluble polysaccharides isolated from Panax ginseng C. A. Meyer. Journal of ethnopharmacology. Jul 20 2010;130(2):421-3.
92. Kim HG et al. Antifatigue effects of Panax ginseng C.A. Meyer: a randomised, double-blind, placebo-controlled trial. PLoS One. 2013;8(4):e61271.
93. Sung WS et al. Efficacy of Korean red ginseng (Panax ginseng) for middle-aged and moderate level of chronic fatigue patients: A randomized, double-blind, placebo-controlled trial. Complementary therapies in medicine. Jan 2020;48(October 2019):102246.
94. Ishaque S et al. Rhodiola rosea for physical and mental fatigue: a systematic review. BMC Complement Altern Med. May 29 2012;12(1):70.
95. Mao JJ et al. Rhodiola rosea versus sertraline for major depressive disorder: A randomized placebo-controlled trial. Phytomedicine. Mar 15 2015;22(3):394-9.
96. Singh N et al. An overview on ashwagandha: a Rasayana (rejuvenator) of Ayurveda. African journal of traditional, complementary, and alternative medicines: AJTCAM / African Networks on Ethnomedicines . 2011;8(5 Suppl):208-13.
97. Kulkarni SK et al. Withania somnifera: an Indian ginseng. Progress in neuro-psychopharmacology & biological psychiatry. Jul 1 2008;32(5):1093-105.
98. Biswal BM et al. Effect of Withania somnifera (Ashwagandha) on the development of chemotherapy-induced fatigue and quality of life in breast cancer patients. Integrative cancer therapies. Jul 2013;12(4):312-22.
参考来源:
美国疾控中心CDC
http://www.cdc.gov
美国CFS网
http://solvecfs.org
美国国立公众健康网
www.medlineplus.gov
加拿大公众卫生局
http://www.phac-aspc.gc.ca
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

